Понимание дипольного момента и полярности молекул для глубокого анализа веществ
Дипольный момент и полярность молекулы — важные характеристики, определяющие взаимодействие молекул между собой. Эти параметры влияют на растворимость веществ, их химическую активность, а также на многие другие физико-химические свойства. Понимание этих понятий помогает в изучении молекулярной структуры и поведения различных веществ в различных условиях.


При изучении полярности молекул важно учитывать их симметрию, поскольку симметричные молекулы часто оказываются неполярными, даже если атомы внутри них имеют разные электроотрицательности.

ЧК_МИФ 3_3_4_(L3) Поляризац3ия молекул диэлектрика

Изучение дипольного момента помогает прогнозировать поведение молекул в электрических и магнитных полях, что полезно для разработки новых материалов и технологий.
Поляризация молекул, ч 1

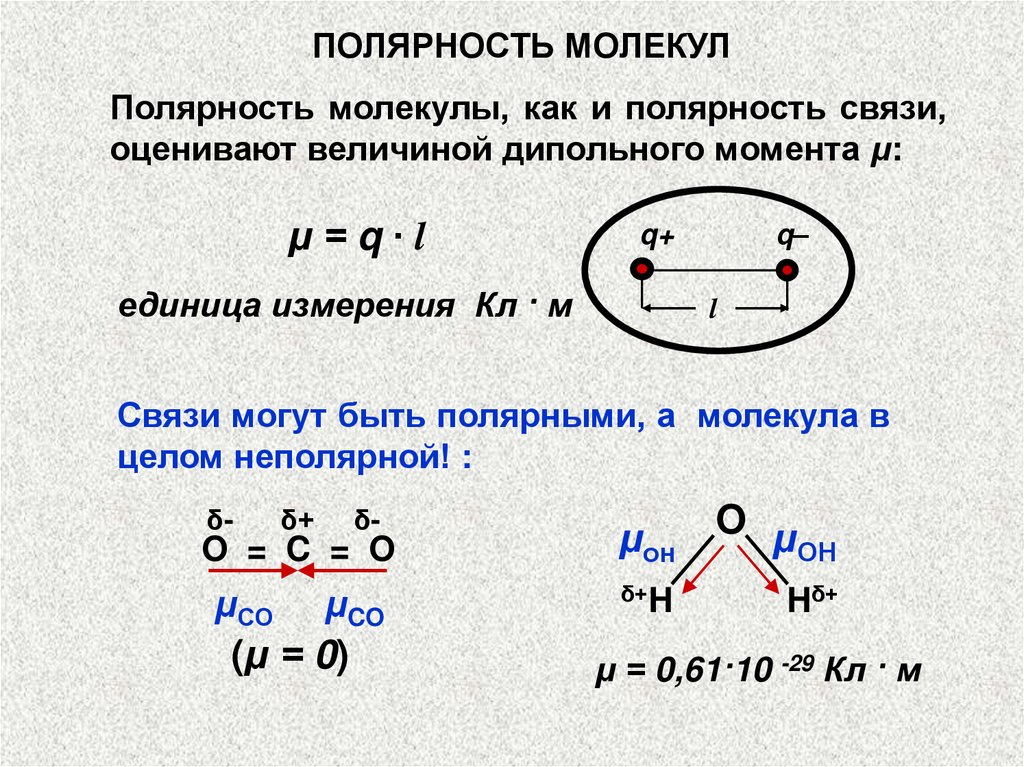
Для определения полярности молекулы можно использовать понятие электроотрицательности атомов: чем большая разница в электроотрицательности, тем более полярной будет молекула.

Готовимся к ЕГЭ по химии с нуля. Полярность молекул и связей.
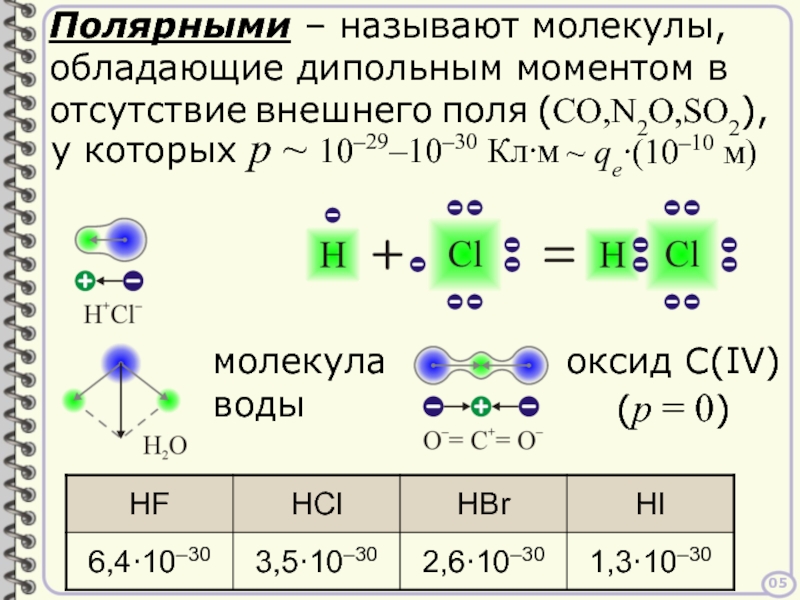
Если молекула обладает высокоэлектронной плотностью на одном конце и дефицитом на другом, она будет иметь дипольный момент, что влияет на ее межмолекулярные взаимодействия.
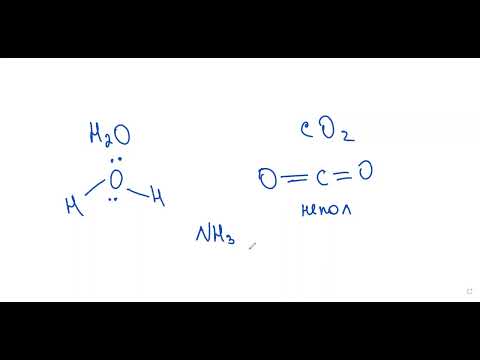
Полярность молекул
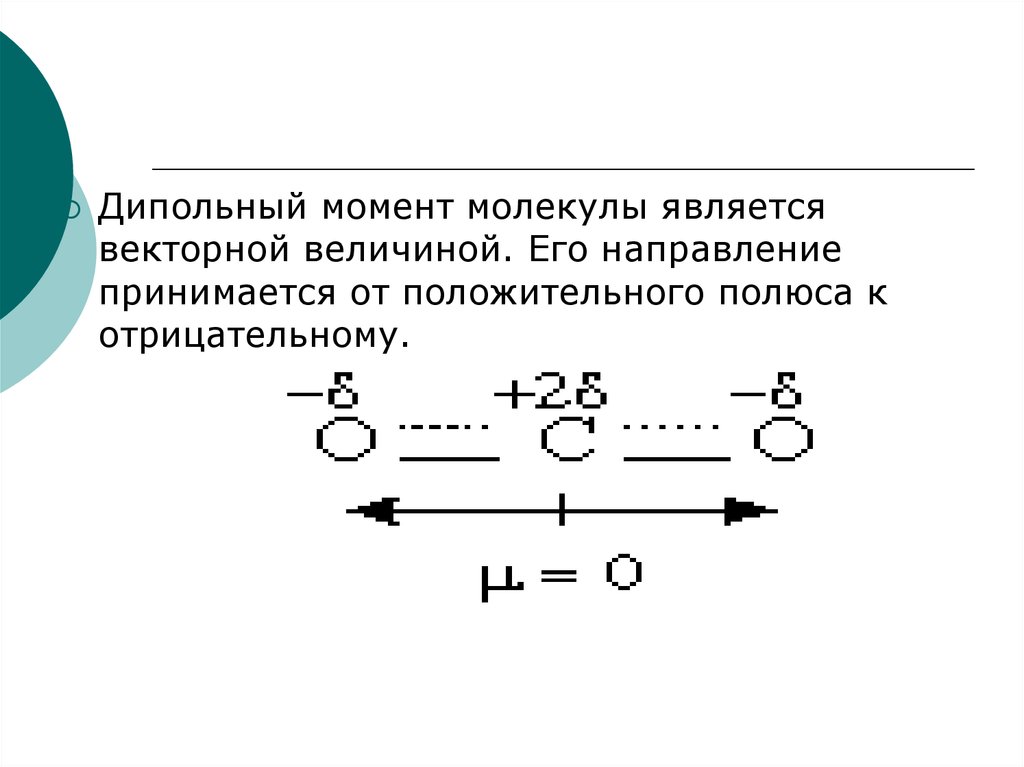
Внимание к дипольному моменту особенно важно в контексте химии растворителей, так как полярные растворители могут лучше растворять полярные вещества.
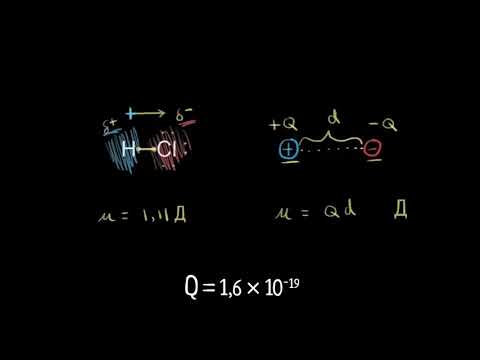
Дипольный момент (видео 26) - Химические связи и структура молекул - Химия

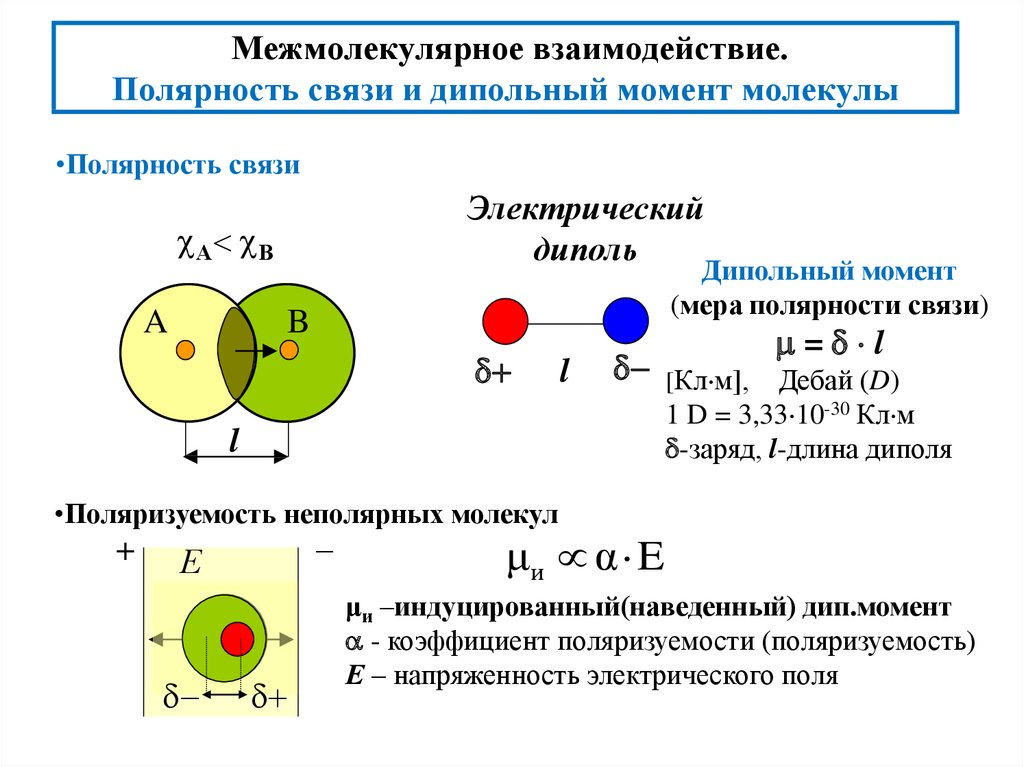
При наличии нескольких дипольных моментов в молекуле важно учитывать их векторную сумму для точного анализа полярности молекулы в целом.
Если молекула имеет симметричную форму, как углеродный диоксид (CO2), несмотря на наличие полярных связей, она будет неполярной.

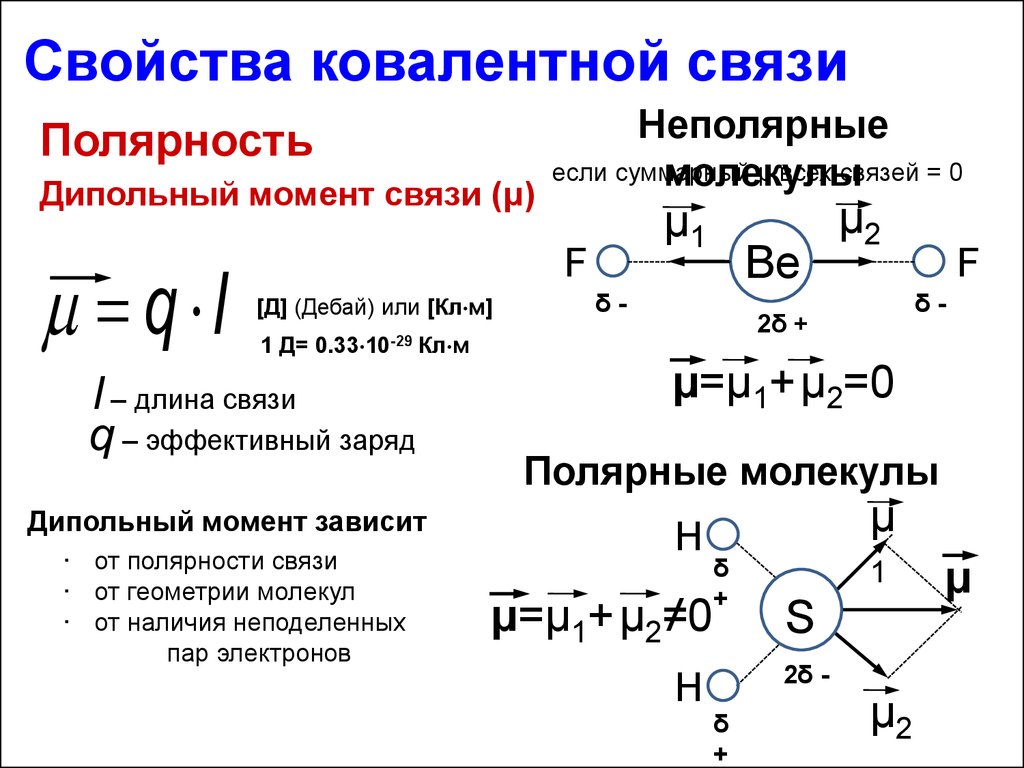
Для молекул с различными типами связей (ионными и коволентными) важно учитывать, как их полярности взаимодействуют друг с другом, что может менять общую полярность молекулы.

Демонстрация: Генератор Ван де Граафа

Поляризация света, 1981
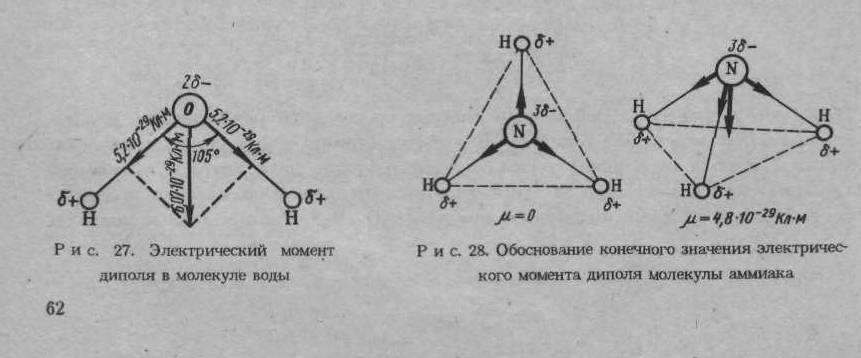
При изучении диэлектрической проницаемости веществ полезно учитывать их дипольный момент, так как молекулы с большим дипольным моментом будут более поляризуемыми в электрическом поле.
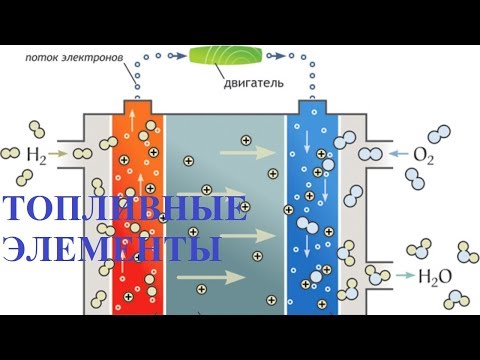
ТОПЛИВНЫЕ ЭЛЕМЕНТЫ
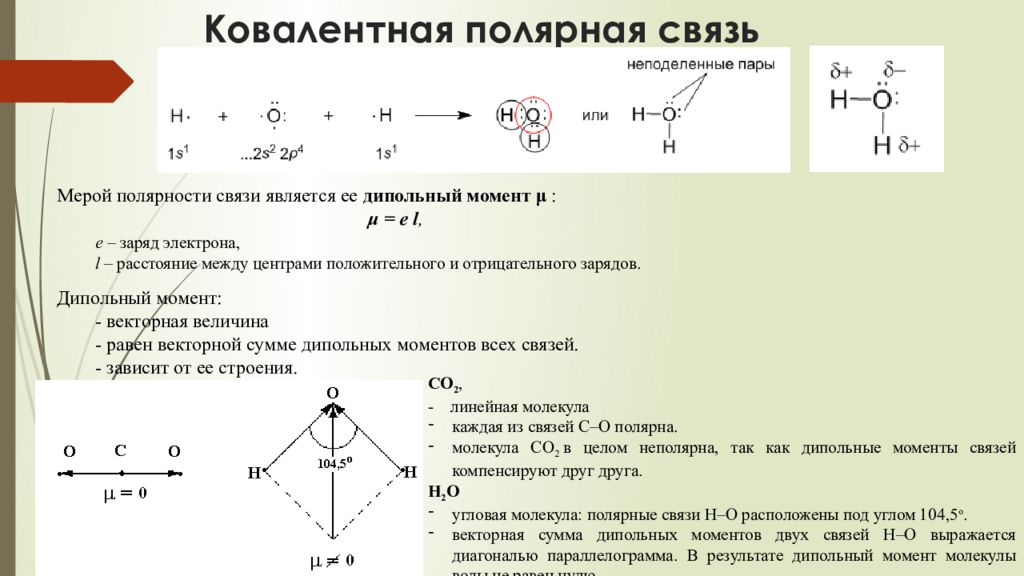
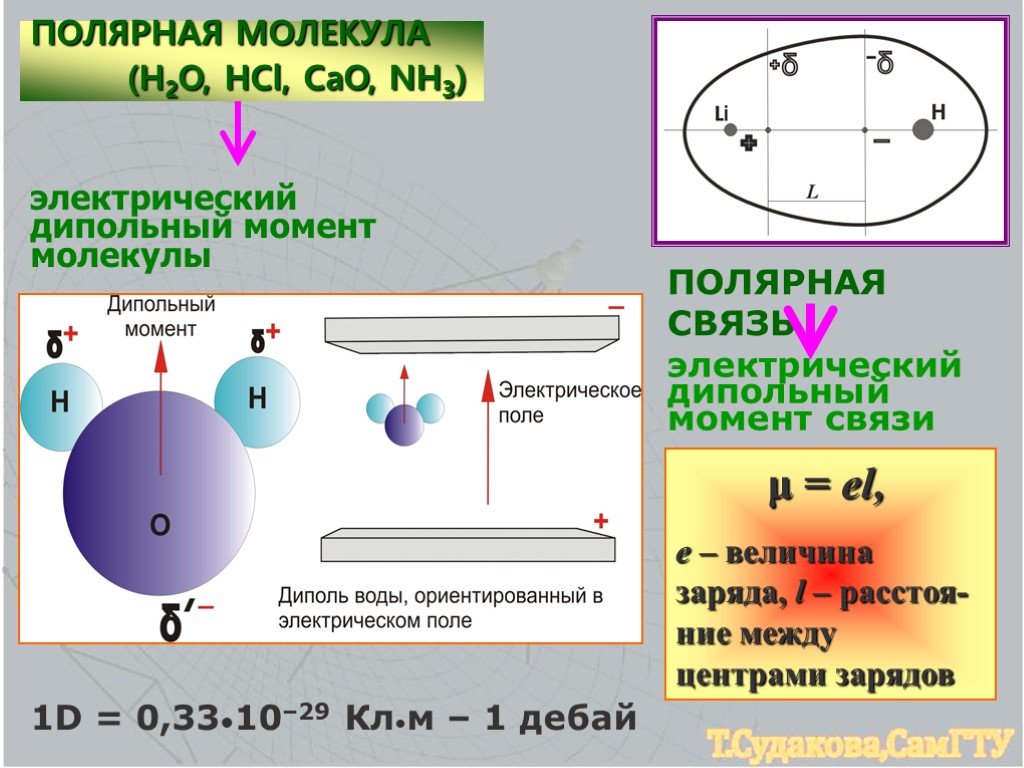
Для понимания взаимодействий в химических реакциях важно учитывать полярность молекул, так как она определяет их способность к образованию водородных связей и другим типам слабых взаимодействий.

Как отличать полярные молекулы от неполярных? Дипольный момент.