Как понять и применить законы термодинамики для самопроизвольных процессов
На этой странице вы найдете подборку полезных советов и фотографий, которые помогут разобраться в условиях протекания самопроизвольных процессов в термодинамике и понять их практическое значение.


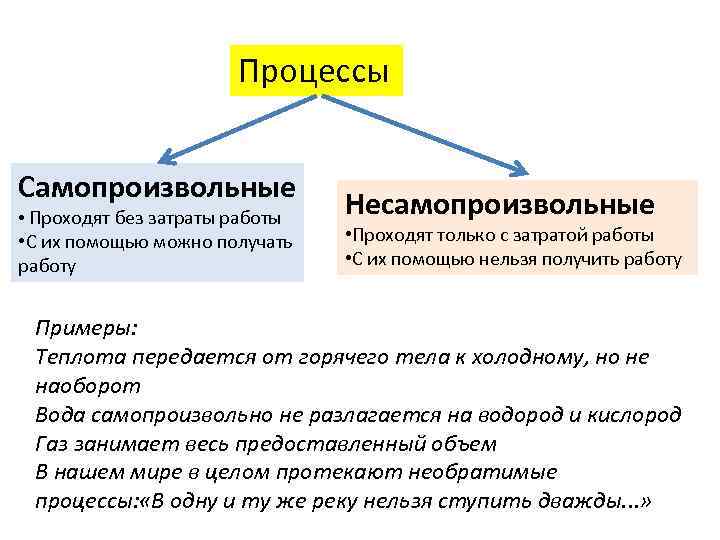
Изучите второй закон термодинамики, так как он определяет направление самопроизвольных процессов.
1. ЭЛЕМЕНТЫ ТЕРМОДИНАМИКИ И КИНЕТИКИ - ВВЕДЕНИЕ


Обратите внимание на изменение энтропии: она увеличивается в самопроизвольных процессах в замкнутой системе.

Химия - Тепловой эффект химической реакции (энтальпия)

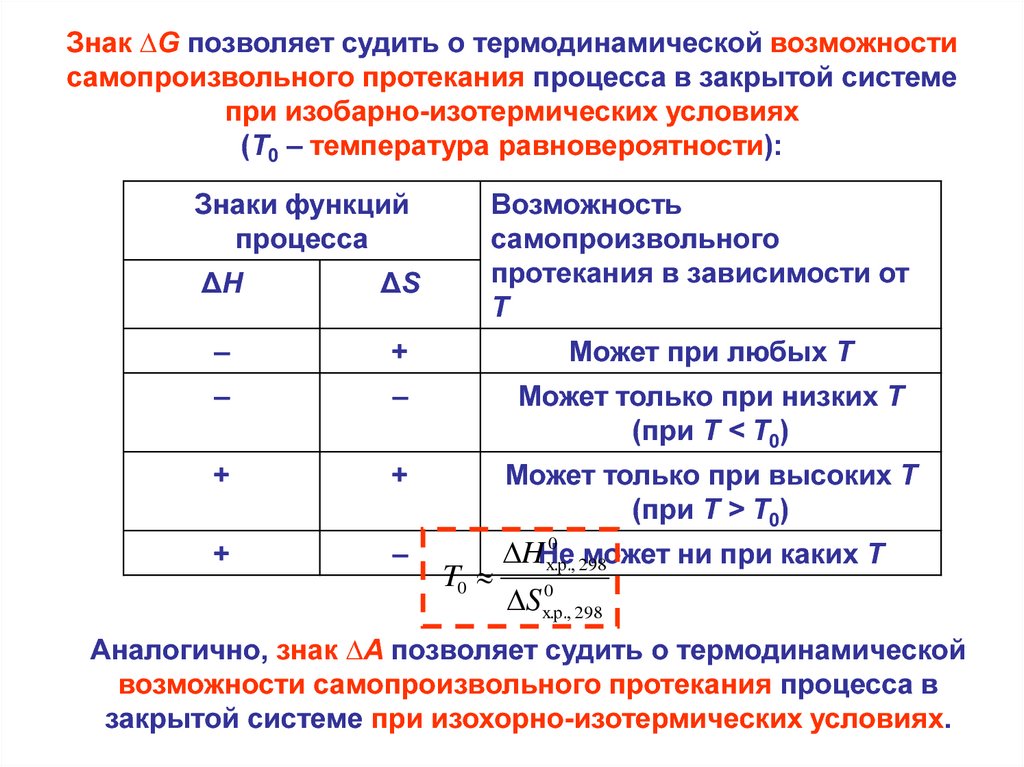
Помните, что уменьшение энергии Гиббса указывает на самопроизвольность процесса.

Обратимые и необратимые процессы. Энтропия. Второй закон термодинамики. 10 класс.

Используйте диаграммы состояния для визуального анализа термодинамических процессов.

Второе начало термодинамики


Всегда учитывайте условия температуры и давления, они влияют на направление процессов.
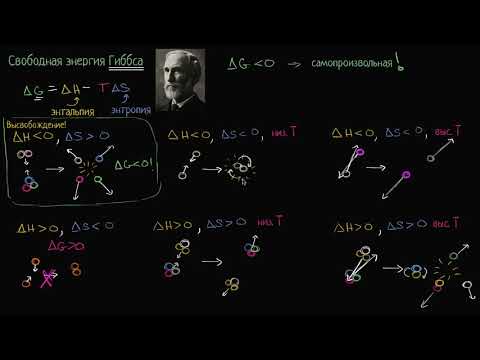
Свободная энергия Гиббса и самопроизвольные реакции (видео 8) - Энергия- Биология

Изучите примеры реальных процессов, таких как теплопередача или химические реакции, чтобы лучше понять теорию.

Применяйте математические модели для расчета энергии Гельмгольца и Гиббса.

Разберитесь в понятии равновесия: оно достигается, когда система перестает изменяться со временем.

Энтропия и второй закон термодинамики (видео 6) - Энергия- Биология
Проверьте, учитываются ли в расчетах как внешние, так и внутренние факторы.

Используйте доступные симуляции и программные инструменты для анализа термодинамических процессов.


Физиология обмена веществ и энергии. Терморегуляция