Как изменение условий влияет на равновесие в процессе гидролиза
Гидролиз — это процесс, при котором вода взаимодействует с веществом, вызывая его распад на более простые компоненты. Одним из ключевых аспектов гидролиза является изменение химического равновесия, которое может смещаться в зависимости от различных факторов. Важно понимать, как различные условия, такие как температура, концентрация или добавление кислот и оснований, могут повлиять на это равновесие. Эта подборка поможет вам разобраться в том, как управлять этим процессом в лабораторных и практических условиях.
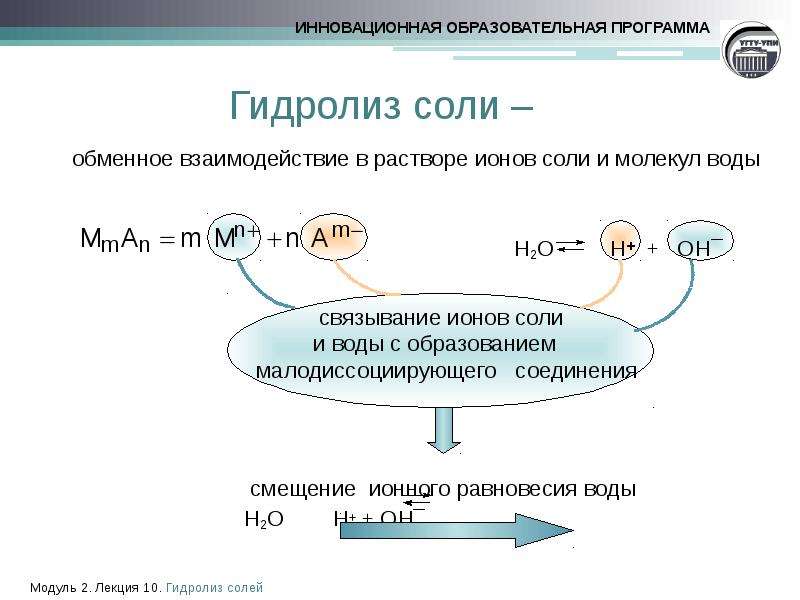
Для успешного контроля над процессом гидролиза важно учитывать pH раствора, так как изменения кислотности могут значительно смещать равновесие реакции.

Смещение химического равновесия - ЭКСПЕРИМЕНТЫ
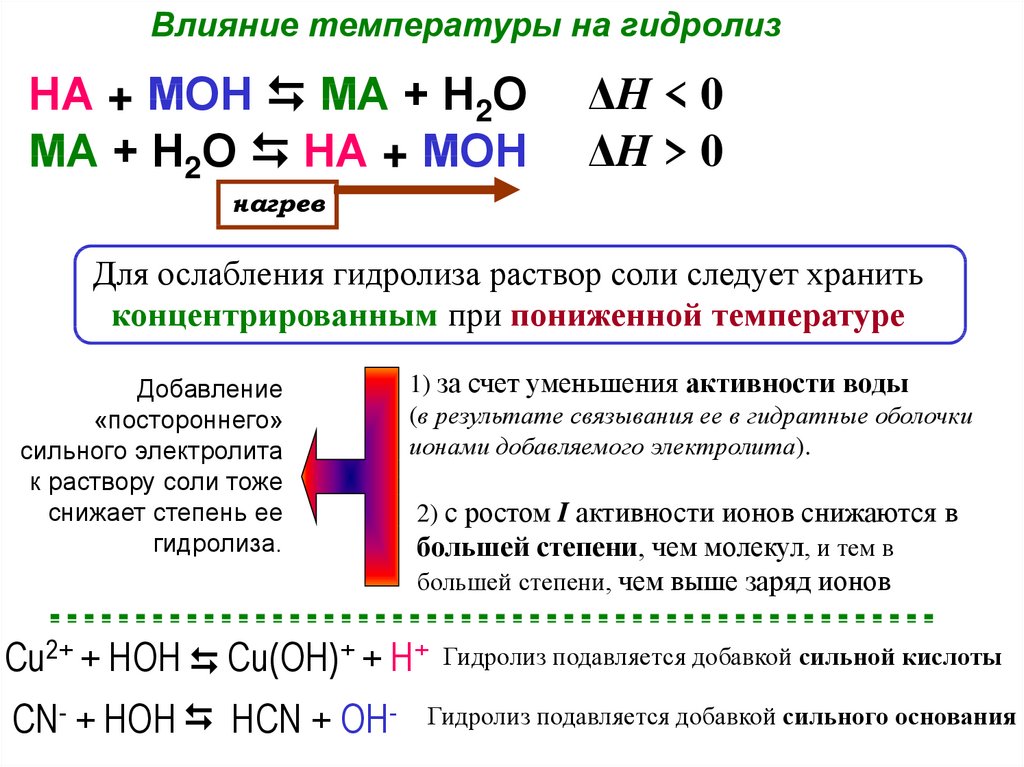

При увеличении температуры скорость гидролиза обычно повышается, но не забывайте, что это может привести к изменению равновесия в сторону образования определённых продуктов.

H2O + S^2- = OH^- + HS^- ХИМИЯ ЕГЭ 2024 Типовое задание 22 Смещение химического равновесия Гидролиз

Для изменения направления реакции гидролиза можно использовать добавление слабых кислот или оснований, что изменит концентрацию ионных веществ в растворе.

ВСЁ О ХИМИЧЕСКОМ РАВНОВЕСИИ для ЕГЭ за 15 минут - Химия ЕГЭ УМСКУЛ

Важно проводить эксперименты с контролируемыми условиями, чтобы точно изучить, как разные факторы, такие как концентрация реагентов и температура, влияют на равновесие.

Всё о ГИДРОЛИЗЕ для ЕГЭ по химии - задание №21

Применение катализаторов в реакции гидролиза может ускорить процесс, но не изменит положения равновесия, позволяя исследовать его более эффективно.
Условия смещения химического равновесия. 9 класс.

Если вам нужно усилить или ослабить гидролиз, попробуйте изменить растворимость веществ, так как это также может повлиять на соотношение продуктов и реагентов.
Следите за количеством воды в системе: если воды недостаточно, процесс гидролиза может остановиться из-за нехватки растворителя.

Обратимые и необратимые реакции - Химическое равновесие и условия его смещения

Взаимодействие с солями может изменить концентрацию ионов, что повлияет на смещение равновесия в сторону либо продуктов, либо исходных веществ.
Для предсказания направления реакции гидролиза используйте принципы химической термодинамики, такие как изменение свободной энергии Гиббса.


При планировании эксперимента по гидролизу учитывайте влияние давления, особенно в случае газообразных продуктов, так как это может значительно повлиять на равновесие реакции.


Гидролиз солей: Вся теория и практика для задания 21 ЕГЭ по химии