Основы теории 1 моля идеального газа: важные моменты и советы для изучения
1 моль идеального газа — это важная величина, которая используется в термодинамике для описания поведения газа при различных условиях. Этот концепт помогает лучше понять взаимодействие молекул, а также свойства газа в различных физических процессах. Изучение этой темы необходимо для решения задач по физике и химии, связанных с идеальными газами.


Не забывайте, что 1 моль идеального газа при стандартных условиях занимает объём 22,4 литра.

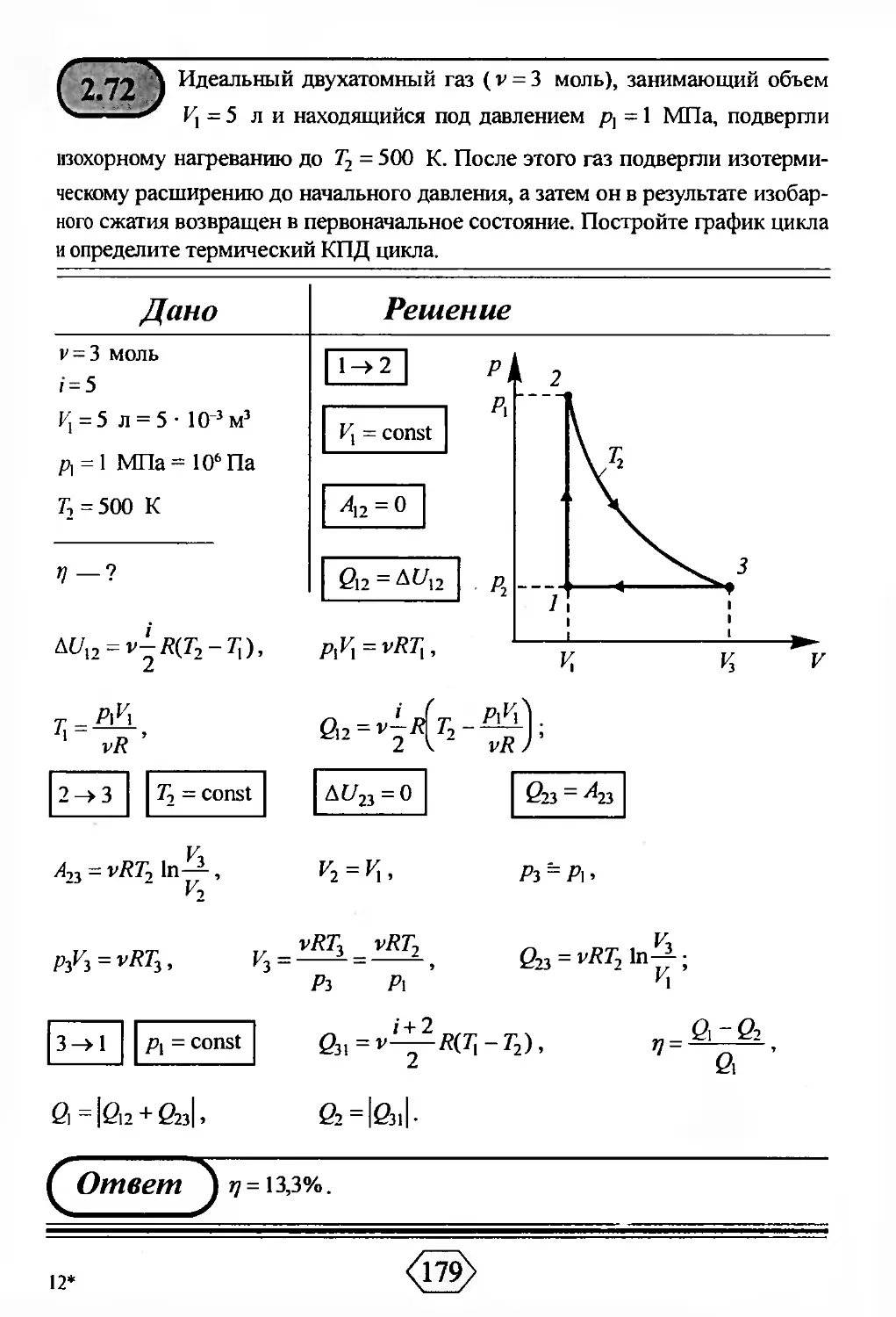
В результате изохорного перехода 1 моль идеального газа из начального состояния в конечное - №
При расчётах помимо идеального газа учитывайте погрешности, связанные с реальными условиями, такими как давление и температура.

Все типы 7 задание газ и изопроцессы - Физика ЕГЭ 2025


Запомните основные уравнения состояния идеального газа, например, уравнение Бойля-Мариотта и уравнение состояния для изотермического процесса.

Борщевский А.Я. - Физическая химия - 1. Введение в курс. Понятия идеального и реального газов
Для решения задач важно точно учитывать температуру и давление, так как они напрямую влияют на объём газа.
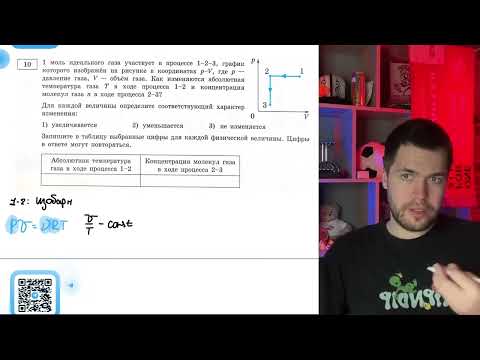
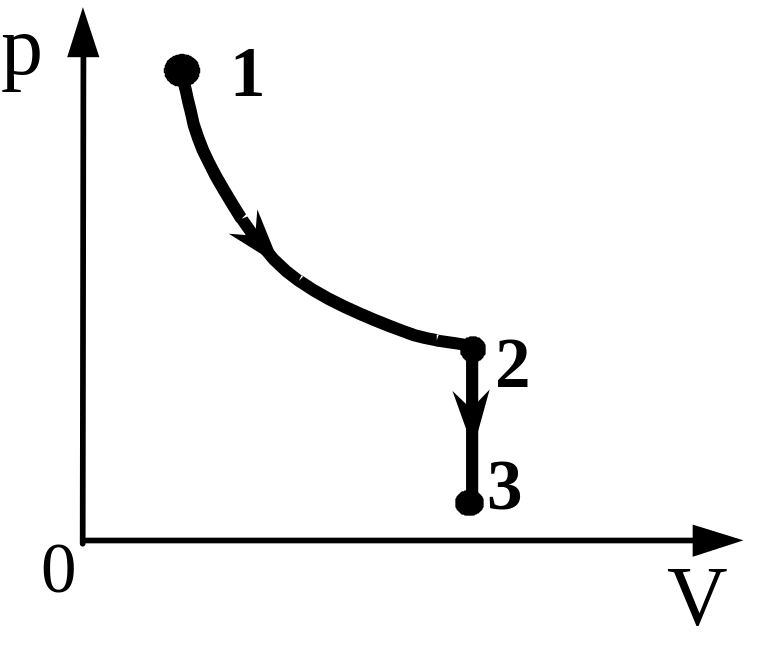
1 моль идеального газа участвует в процессе 1—2—3, график которого изображён на рисунке - №

Используйте форму записи уравнений для молекулярной массы газа, что помогает при расчёте количества вещества и молекул.
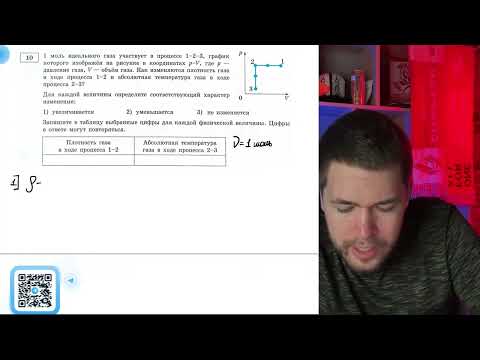
1 моль идеального газа участвует в процессе 1—2—3, график которого изображён на рисунке - №


Важно помнить, что при повышении температуры давление газа будет увеличиваться, если объём остается постоянным.
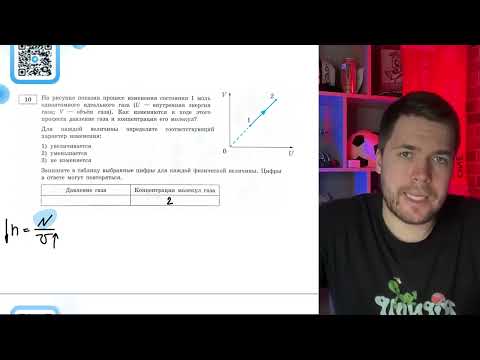
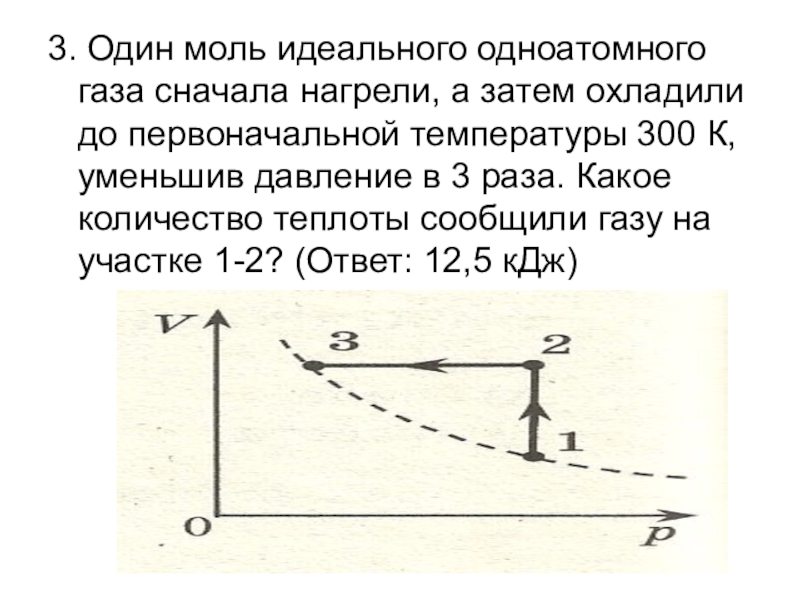
На рисунке показан процесс изменения состояния 1 моль одноатомного идеального газа (U внутренняя - №

Не забывайте про коэффициент адиабаты, который влияет на изменение состояния газа при адиабатном процессе.

Для более точных вычислений всегда проверяйте единицы измерений, чтобы избежать ошибок при подставлении значений в уравнения.
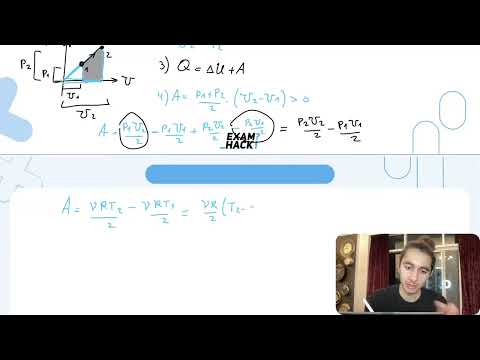
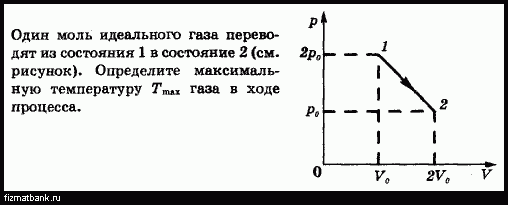
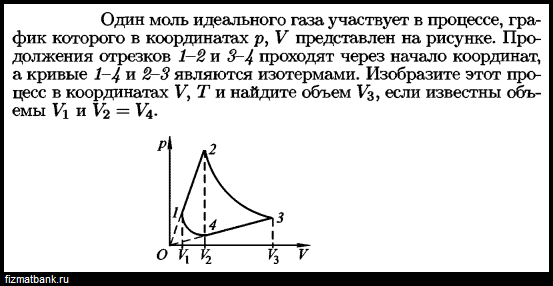
Один моль одноатомного идеального газа переводят из состояния 1 в состояние 2 таким - №29408

Изучая свойства идеальных газов, учитывайте, что молекулы газа не взаимодействуют друг с другом, что делает их поведение проще для анализа.


Для успешного решения задач по идеальному газу важно не только запомнить теорию, но и хорошо понимать практические аспекты её применения.
