Таблица Полинга: ключевые моменты для понимания электроотрицательности элементов и их влияния на химические реакции
Электроотрицательность элементов — важный фактор в химии, влияющий на формирование химических связей. В этой подборке мы объясним, как использовать шкалу относительной электроотрицательности Полинга для анализа и предсказания свойств различных веществ. Таблица Полинга поможет вам разобраться в тонкостях химии и эффективно применять знания на практике.

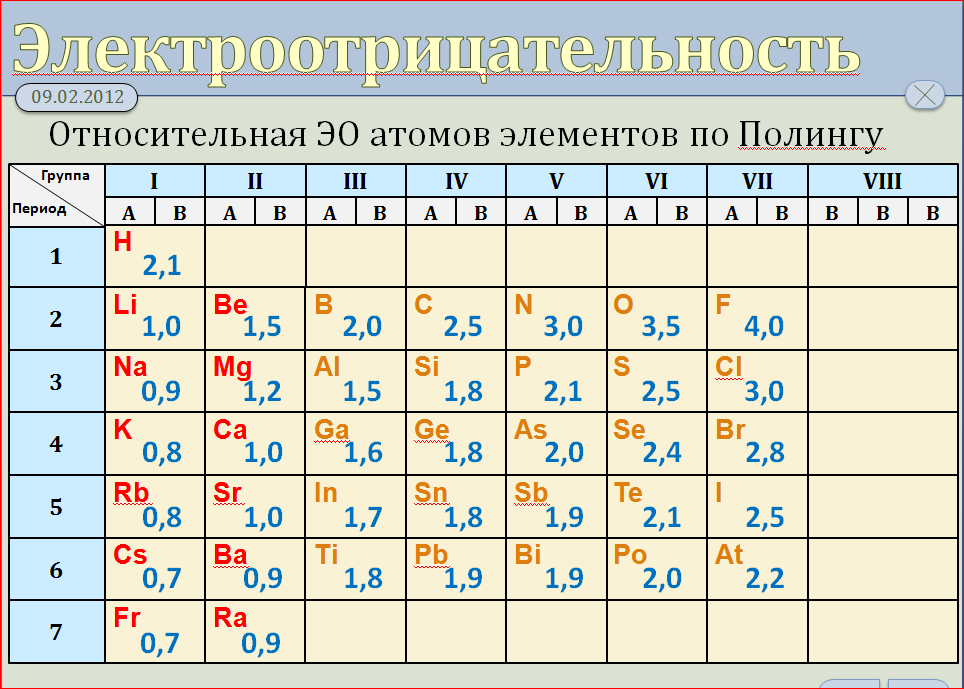
Запоминайте, что элементы с высокой электроотрицательностью легко притягивают электроны, что влияет на полярность химических связей.

222. Шкала относительной электроотрицательности Полинга
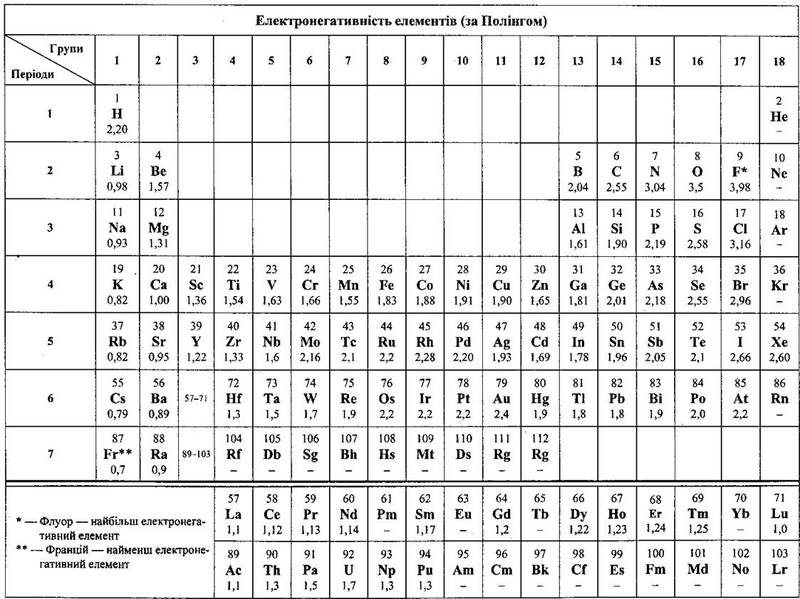
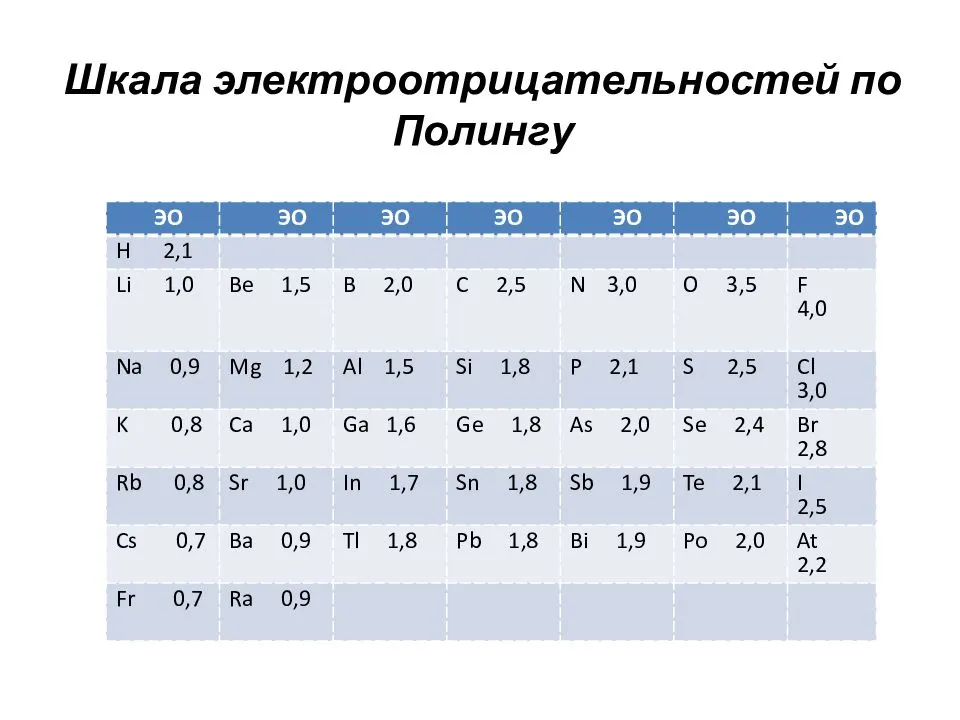
Для того чтобы предсказать тип связи между атомами, сравните их электроотрицательности: если разница велика, то связь ионная, если мала — ковалентная.

8 Класс. Распределение электронов в атоме - Электронные формулы - ПОЙМЁТ КАЖДЫЙ

Используйте таблицу Полинга для определения кислотных и основных свойств соединений, так как электроотрицательность элементов играет ключевую роль в этих процессах.

Понятие электроотрицательности, 8 класс
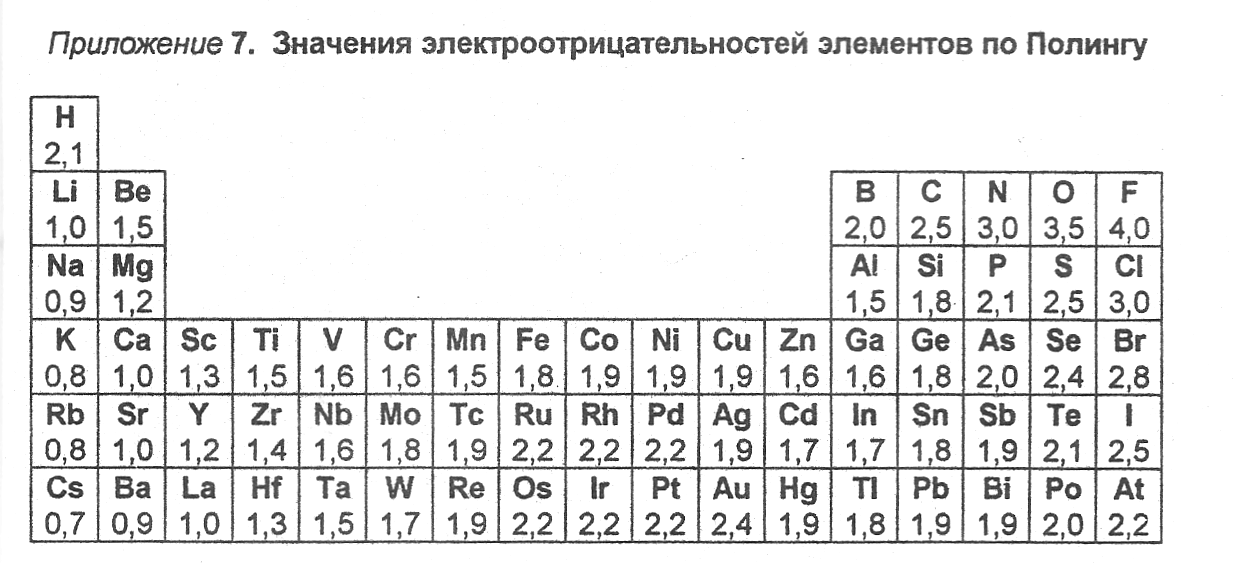
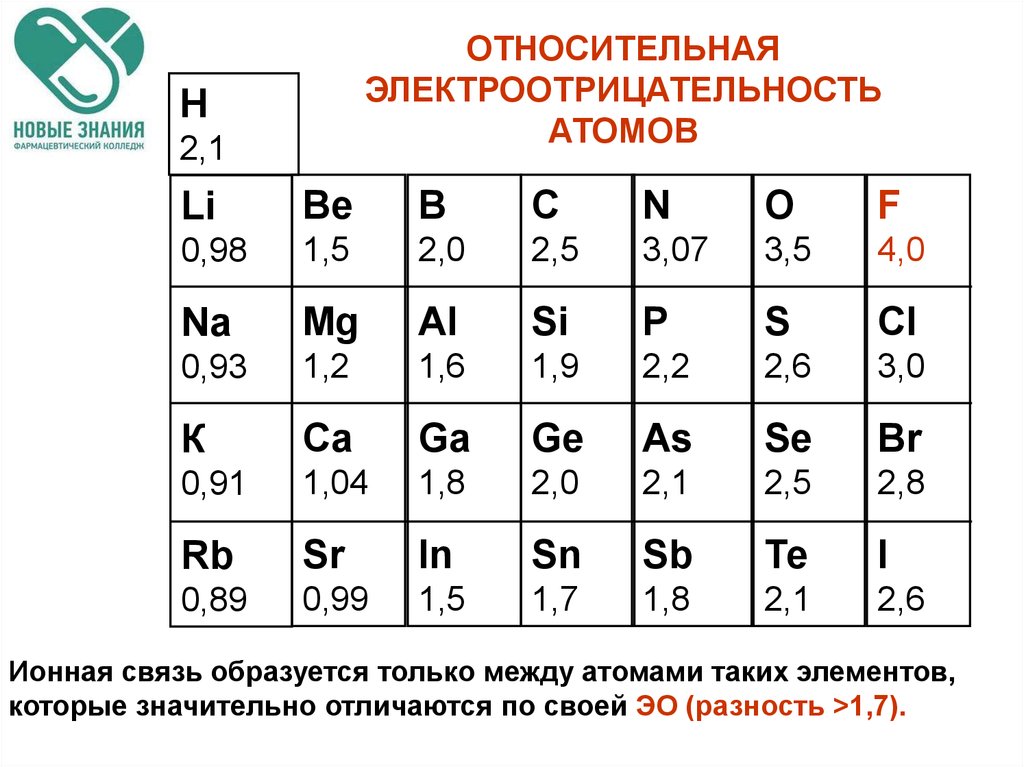
Учтите, что элементы с низкой электроотрицательностью, как правило, образуют металличные связи, а высокоэлектроотрицательные — ковалентные и ионные.
электроотрицательность задания/8 класс

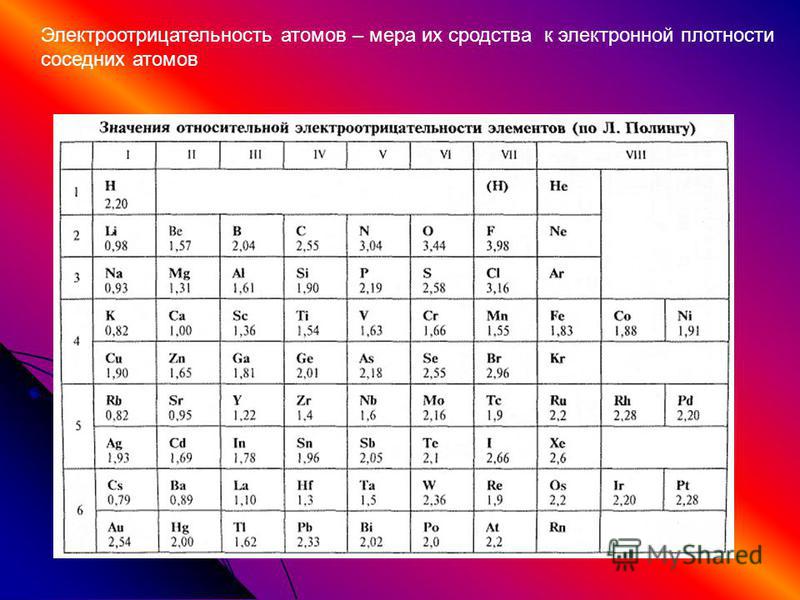
При изучении таблицы Полинга помните, что электроотрицательность увеличивается по мере продвижения от левого нижнего угла таблицы к правому верхнему.

8 класс. Электроотрицательность химических элементов


Для определения полярности молекул используйте разницу в электроотрицательности атомов — это поможет понять, будет ли молекула полярной или неполярной.
Следите за тем, чтобы правильно интерпретировать данные о электроотрицательности, так как иногда маленькие различия могут сильно повлиять на свойства вещества.

Что такое электроотрицательность??

Запомните, что электроотрицательность влияет на растворимость веществ, так как более электроотрицательные молекулы часто лучше растворяются в полярных растворителях.
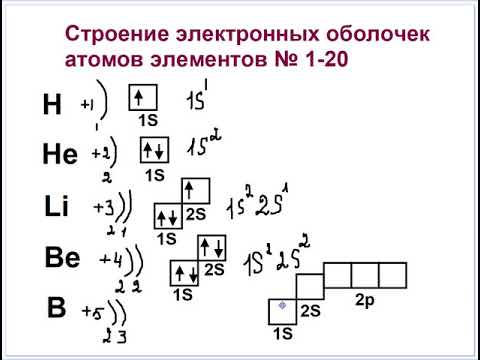
Строение электронных оболочек элементов 1-20


Используйте шкалу Полинга, чтобы понять, какие атомы в молекуле будут иметь большую склонность к образованию водородных связей.


Для точного понимания химических реакций всегда обращайте внимание на электроотрицательность элементов, так как она предсказывает многие реакции и их механизмы.

Электроотрицательность химических элементов. 8 класс.