Пространственная форма ковалентных связей: объяснение и примеры
Пространственная структура ковалентной связи играет ключевую роль в формировании свойств молекул. Разберем геометрию молекул, типы связей и их влияние на химические процессы.
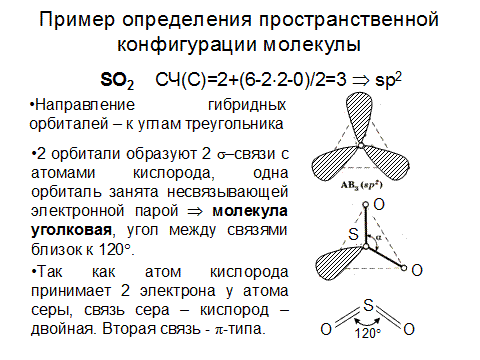
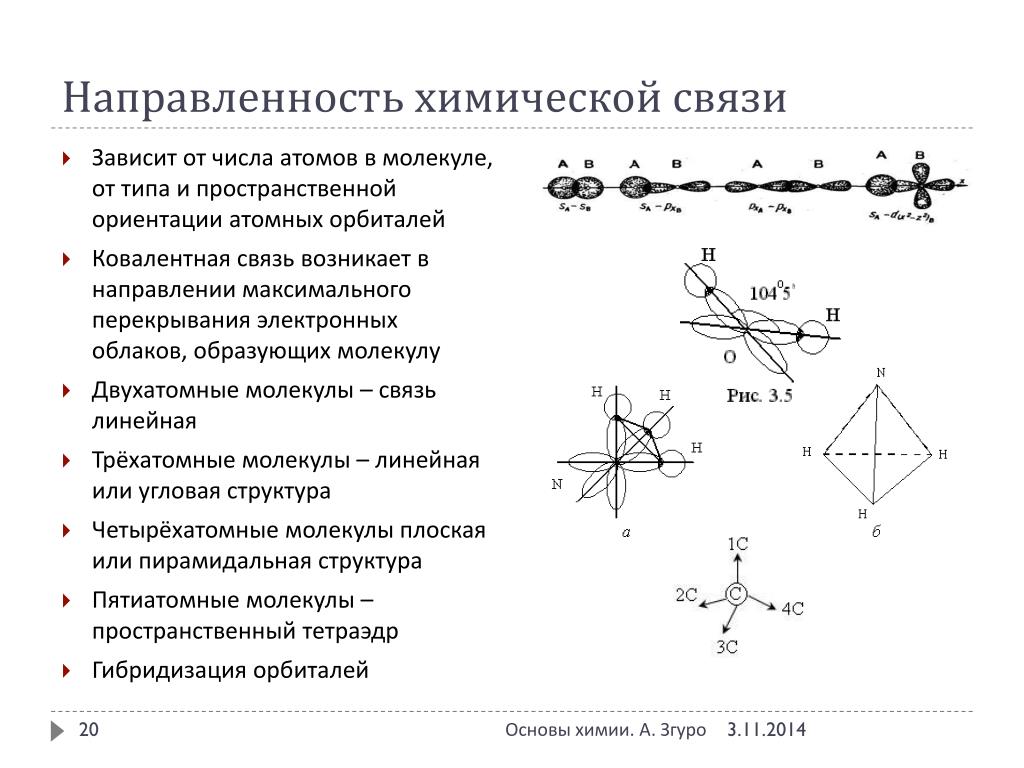
Изучите модель гибридизации орбиталей, чтобы понять, как атомы образуют ковалентные связи.

Ковалентная Полярная Связь — Химическая связь // Химия 8 класс
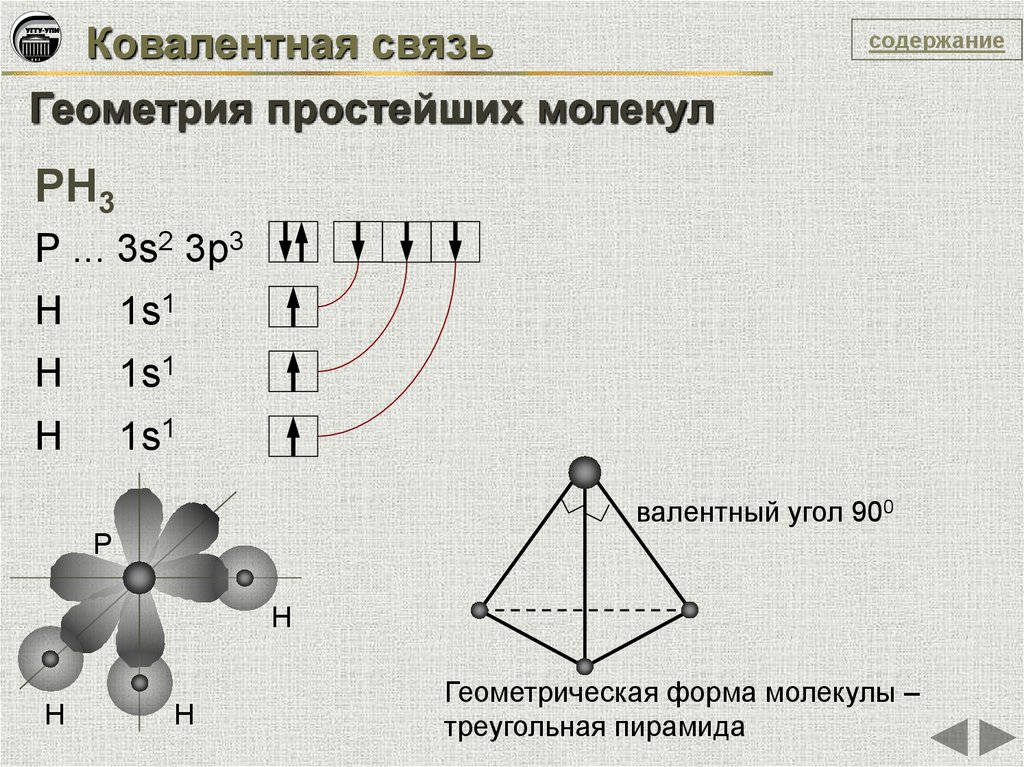
Используйте примеры молекул, такие как H₂O или CH₄, для изучения пространственных структур.

Химическая связь и строение молекул, С.Ю. Шавшукова, профессор кафедры ОАПХ
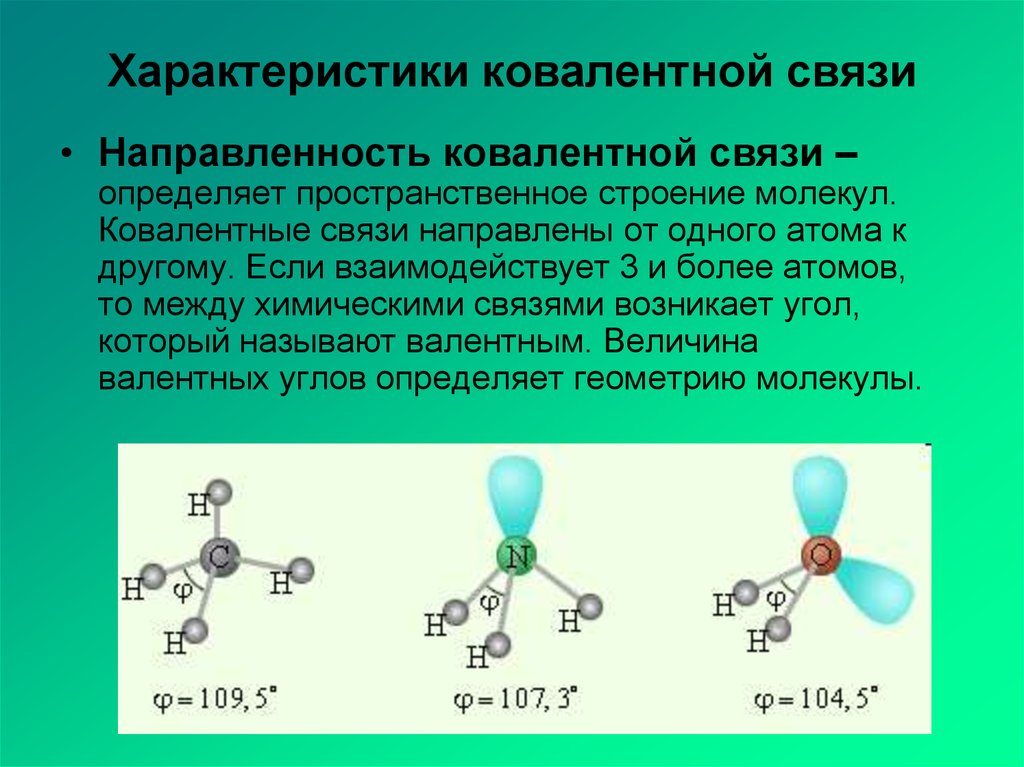
Пользуйтесь электронными формулами, чтобы визуализировать расположение атомов и электронных пар.

57. Механизмы образования ковалентной связи

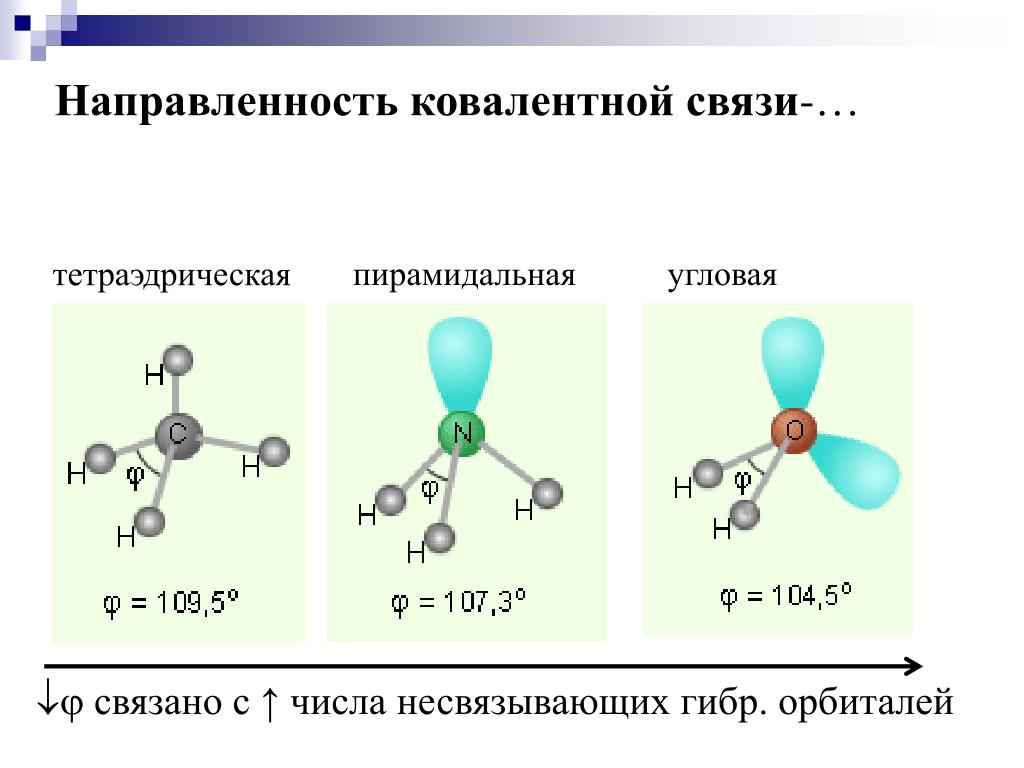
Обратите внимание на угол между связями, например, тетраэдрическую форму в молекулах метана.

Ковалентная Неполярная Связь — Химическая связь // Химия 8 класс
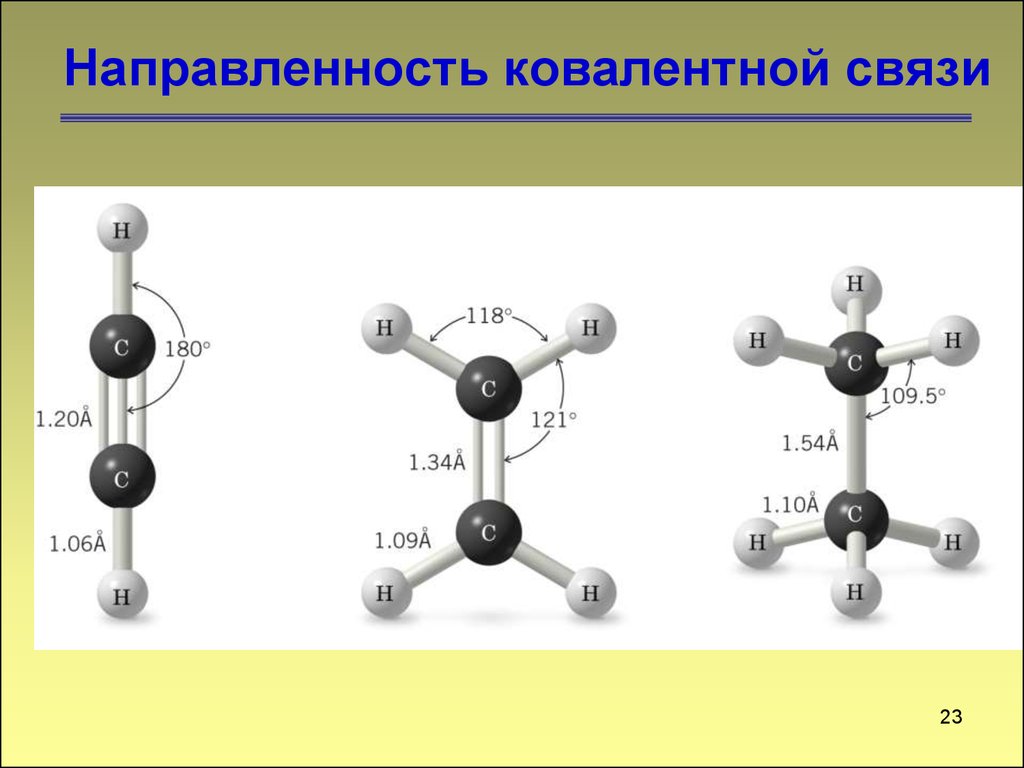
Изучите влияние неподеленных электронных пар на форму молекул, как в случае воды.

Как повысить мощность блока питания - Самое понятное объяснение
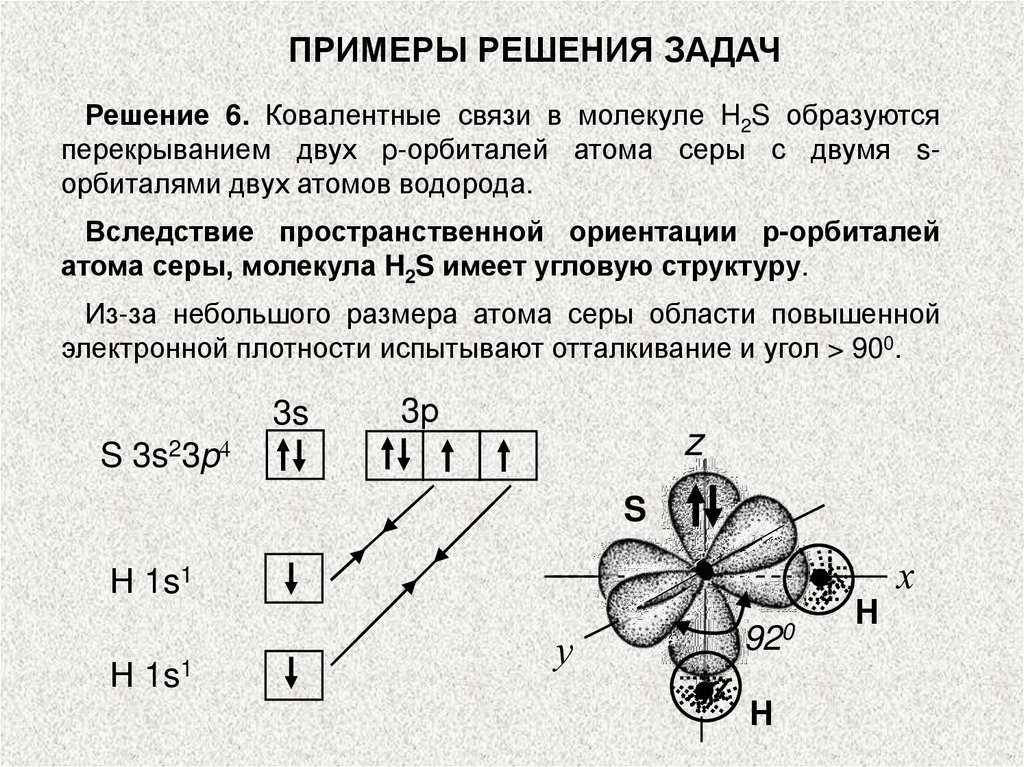
Запомните, что ковалентная связь может быть как полярной, так и неполярной, в зависимости от разницы электроотрицательностей.

Органическая Химия — ЭТО НУЖНО ВИДЕТЬ! Гибридизация орбиталей
Применяйте правила ВСПЕР (теории отталкивания электронных пар) для предсказания формы молекул.


Гибридизация атомных орбиталей и геометрия молекул. 10 класс.
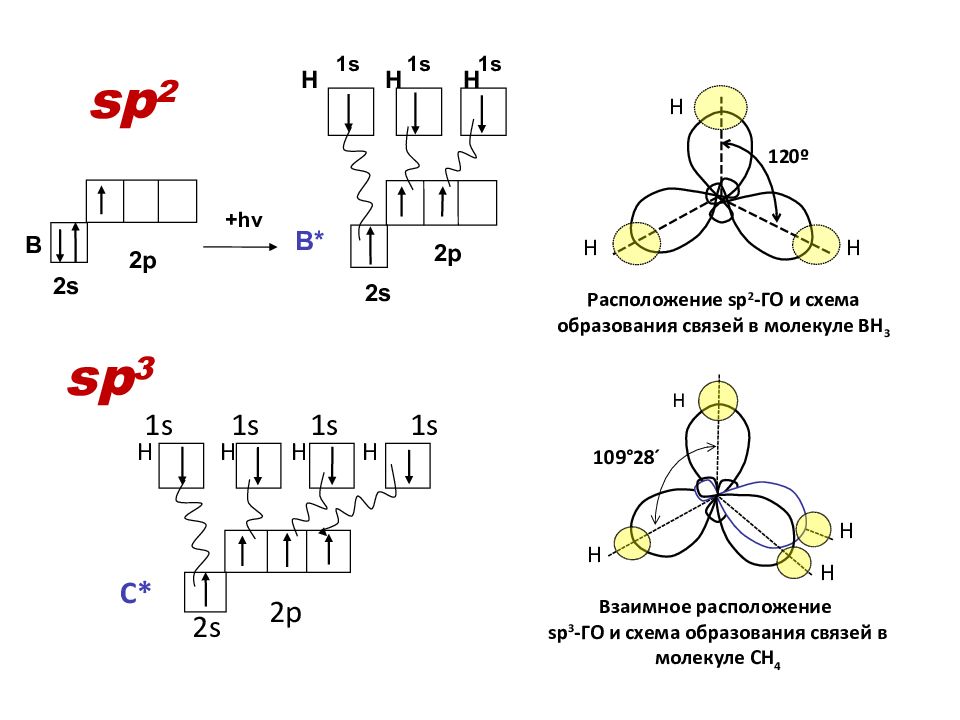
Практикуйтесь в составлении пространственных моделей с помощью химических конструкторов или 3D-программ.
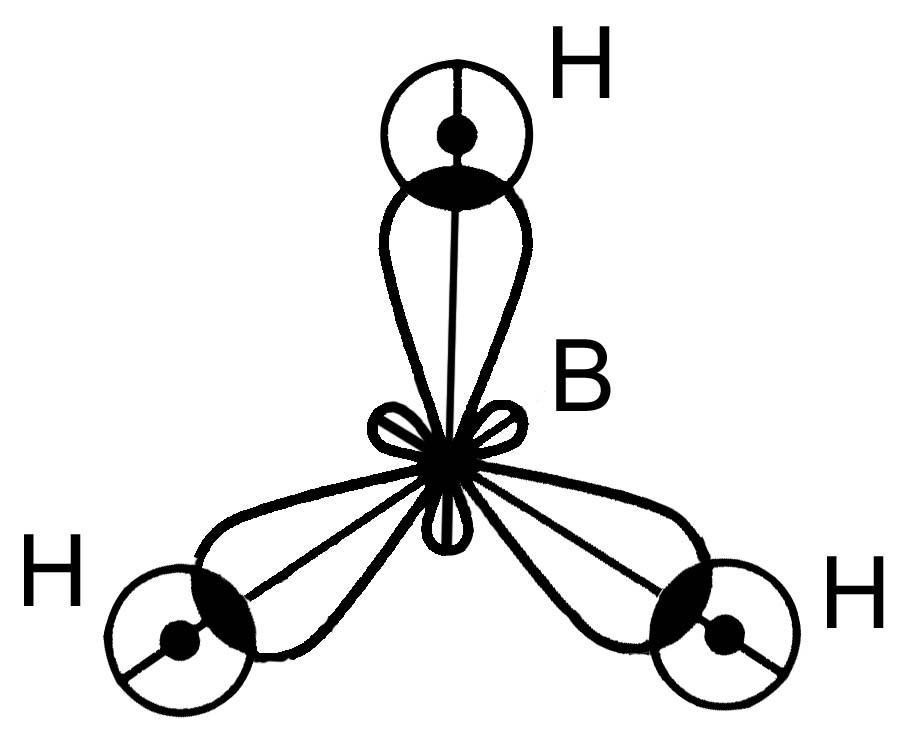
Изучите примеры из органической химии, чтобы увидеть влияние ковалентных связей на свойства веществ.
Ковалентная связь. 8 класс.