Понимание моля вещества: как и зачем рассчитывается 1 моль вещества в химии
Моль вещества — это фундаментальная единица измерения в химии, которая помогает точно определить количество частиц в веществе. Этот показатель крайне важен как для ученых, так и для практических расчетов в разных областях науки. В данной статье мы расскажем, что такое 1 моль, как его вычислять и зачем это нужно, а также приведем полезные советы для работы с мольными расчетами.



Для того чтобы найти массу 1 моля вещества, необходимо умножить его молекулярную массу на число Авогадро, которое равно примерно 6.022×10²³ частиц.

Моль. Молярная масса. Решение задач по химии

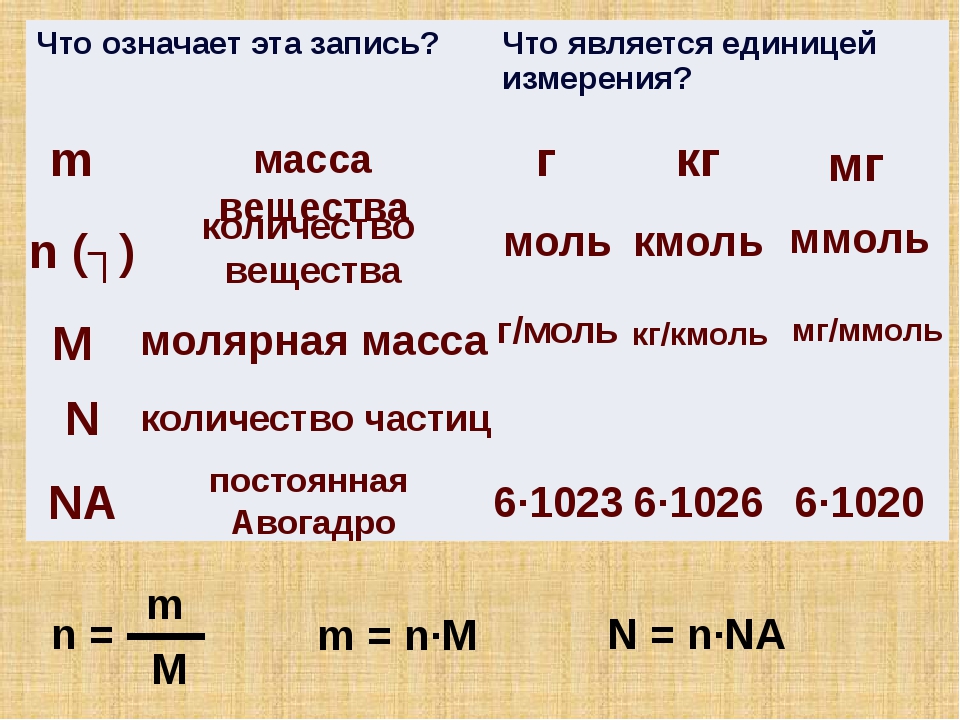
Не забывайте, что 1 моль любого вещества содержит одинаковое количество частиц, независимо от того, о каком веществе идет речь.

МОЛЯРНАЯ МАССА ХИМИЯ // Урок Химии 8 класс: Относительная Молекулярная Масса

При расчетах с мольными массами важно использовать правильные единицы измерения, чтобы не возникло ошибок при вычислениях.

ЧТО ТАКОЕ МОЛЬ И КОЛИЧЕСТВО ВЕЩЕСТВА В ХИМИИ?
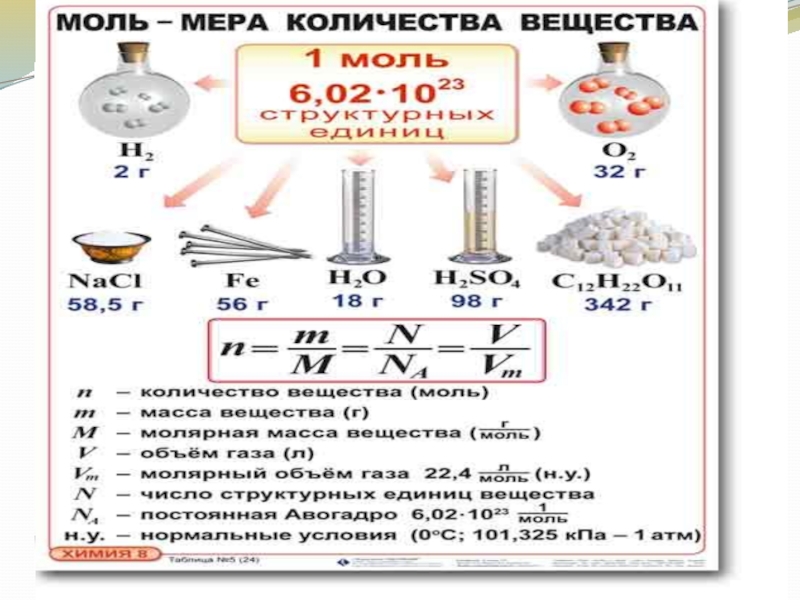
Для точных расчетов массы 1 моля вещества используйте таблицу Менделеева, где указаны атомные массы элементов.

Количество вещества. Моль. Число Авогадро. 8 класс.
Если необходимо найти количество вещества в молях, можно использовать формулу: количество вещества (моли) = масса вещества / молекулярная масса.

Химия. 8 класс. Количество вещества. Моль. Число Авогадро. Молярная масса вещества /18.11.2020/

Для быстрого перехода от массы вещества к молям не забывайте учитывать его плотность, особенно для газов при стандартных условиях.
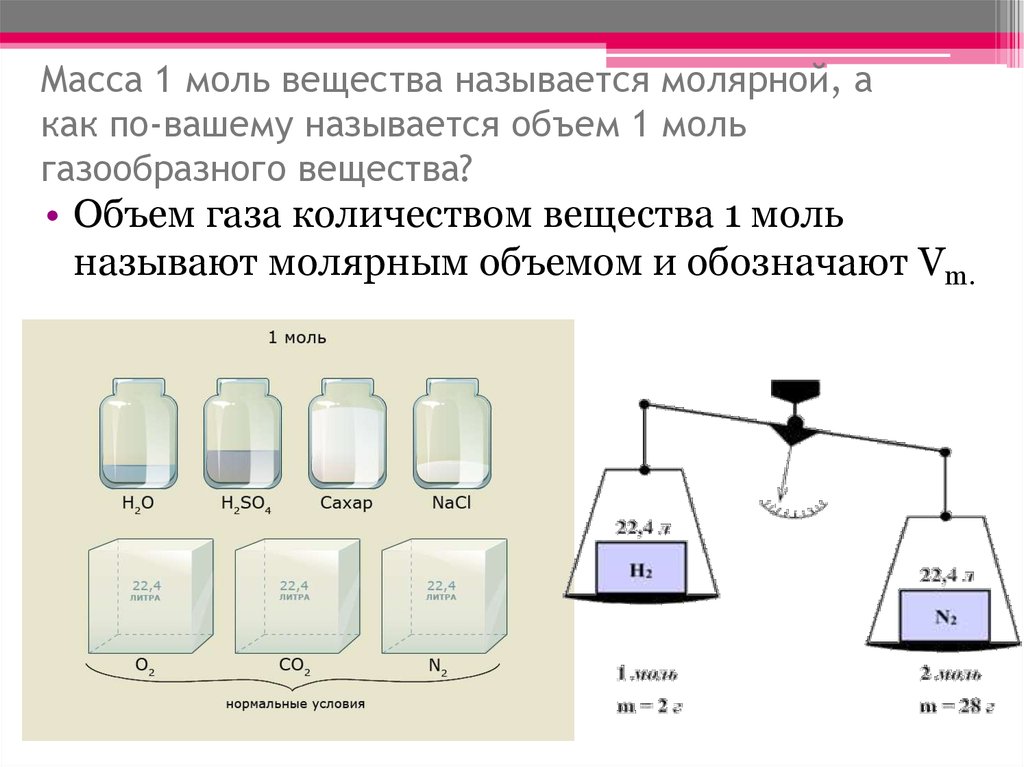
В реальной жизни, например, при приготовлении растворов, часто требуется знание мольных концентраций — это помогает точно подобрать необходимое количество вещества.

Количество вещества. Моль. Число Авогадро. Молярная масса и молярный объем газов - Химия 8 класс

Чтобы упростить молекулярные вычисления в химии, используйте калькуляторы или онлайн-ресурсы для нахождения молей и массы вещества.

Химические задачи: Количество вещества, моль, молярная масса - Химия ОГЭ 2023 - Умскул

Как за 4 МИНУТЫ выучить Химию? Химическое Количество, Моль и Закон Авогадро

Для изучающих химию важно понимать, что 1 моль вещества всегда соответствует его молекулярной массе в граммах — это делает расчеты гораздо проще.

Что такое моль? - Химия - TutorOnline

При работе с мольными расчетами старайтесь не забывать о температурных и давленных условиях, так как они могут влиять на массу вещества, особенно в газообразном состоянии.

Моль. Количество вещества. Химия – просто